欢迎您来到博普特科技官方网站!
 010-82794912
010-82794912
该研究由青岛农业大学团队完成,发表于《Frontiers in Plant Science》,首次整合多光谱成像技术、发芽表型分析与转录组测序,系统探究了人工加速老化条件下两种不同耐储性藜麦品种的种子活力响应机制,揭示了黄酮类生物合成、碳代谢等关键通路及核心基因在种子活力调控中的作用,为藜麦种质资源保存与种子活力改良提供了重要理论依据和分子育种靶点。
文献摘要
种子活力是与种子品质改良及种质资源长期保存密切相关的重要性状,其在储存过程中会逐渐衰退,已成为农业生产中的关键问题。然而,藜麦种子活力衰退的分子调控机制目前仍尚不明确。本研究以两种耐储性差异显著的藜麦品种(Longli No.4(L4)和 Longli No.1(L1))为材料,通过转录组测序解析人工老化条件下与种子活力衰退相关的通路及基因。多光谱成像特征与发芽表型分析显示,L1 种子的活力损失显著低于 L4,表明其具有更强的抗老化能力和耐储性。转录组分析共在 L4 和 L1 中分别鉴定出 272 个和 75 个差异表达基因(DEGs),并揭示了两者代谢通路的差异:L4 种子中黄酮类生物合成、三羧酸循环(TCA 循环)和萜类骨架生物合成通路显著富集,而 L1 种子中碳代谢通路显著富集,涉及 CHS、CHI、AACT、ENO1、IDH、NADP-ME、HAO2L 等关键基因。研究表明,老化对黄酮类和萜类物质的不利影响可能是耐储敏感性种子活力损失更严重的重要原因,而耐储性种子则具有更强的维持碳代谢和能量供应的能力。这些发现阐明了藜麦种子活力衰退的分子机制,也为通过现代分子育种策略改良种子活力提供了新的思路。
研究背景与目的
背景:藜麦是一种营养价值极高的潜力作物,富含优质蛋白、必需氨基酸及生物活性物质,适应多种逆境环境,在粮食安全和产业应用中具有重要地位。但藜麦种子为瘦果型,种皮透气性强、胚乳富含亲水性淀粉,储存过程中易吸水导致活力快速下降,耐储性差,严重制约其生产应用与种质资源长期保存。种子活力是评估种子质量的核心指标,直接影响发芽率、幼苗整齐度及田间成苗率,其衰退机制与遗传背景、代谢通路调控密切相关。已有研究在小麦、水稻等作物中明确了部分与种子活力相关的基因和通路,但藜麦种子活力衰退的分子调控机制尚未明确。人工加速老化是模拟种子自然储存衰退的经典方法,结合多光谱无损检测和转录组分析,可从表型到分子层面系统解析种子活力响应规律,但该技术组合在藜麦中的应用尚未开展。
研究目的:以两种耐储性差异显著的藜麦品种(Longli No.1(L1,高耐储)和 Longli No.4(L4,低耐储))为材料,通过人工加速老化处理,结合多光谱成像和发芽表型分析,明确两者种子活力差异;利用转录组测序筛选老化过程中差异表达基因(DEGs),解析调控种子活力的关键代谢通路;揭示藜麦种子活力衰退的分子机制,为培育高活力、高耐储藜麦品种提供理论支撑。
核心试验方法
①多光谱成像分析:仪器:丹麦 VideometerLab4 多光谱成像系统,涵盖 19 个波段(365-970 nm);分析指标:提取种子面积、长度、宽度、CIELab 颜色参数、饱和度等 14 项形态特征;通过归一化典型判别分析(nCDA)进行种子活力可视化(红色标记高活力种子,蓝色标记低活力种子)。
②发芽表型测定:试验设计:每个处理 3 次重复,每次 50 粒种子,25℃黑暗条件下培养 5 天,每 12 小时记录发芽情况;测定指标:发芽率(GP)、发芽指数(GI)、活力指数(VI),评估种子活力水平。③转录组测序与分析:RNA 提取:采用 Trizol 试剂提取 24 个样本(2 品种 ×4 老化时间 ×3 生物学重复)的总 RNA;测序与比对:构建 cDNA 文库后通过 Illumina HiSeq 4000 测序,clean reads 比对至藜麦参考基因组(ASM168347v1);DEGs 筛选与功能注释:采用 DESeq2 软件筛选 DEGs(|log2FC|≥1 且调整后 P<0.05),通过 GO 和 KEGG 数据库进行功能富集分析;转录因子(TFs)分析:利用 PlantTFDB 4.0 预测差异表达转录因子。
④qRT-PCR 验证:选取 9 个关键 DEGs(涉及黄酮类合成、碳代谢等通路),以 EF1α 为内参基因,采用 2⁻ΔΔCt 法验证转录组结果可靠性。
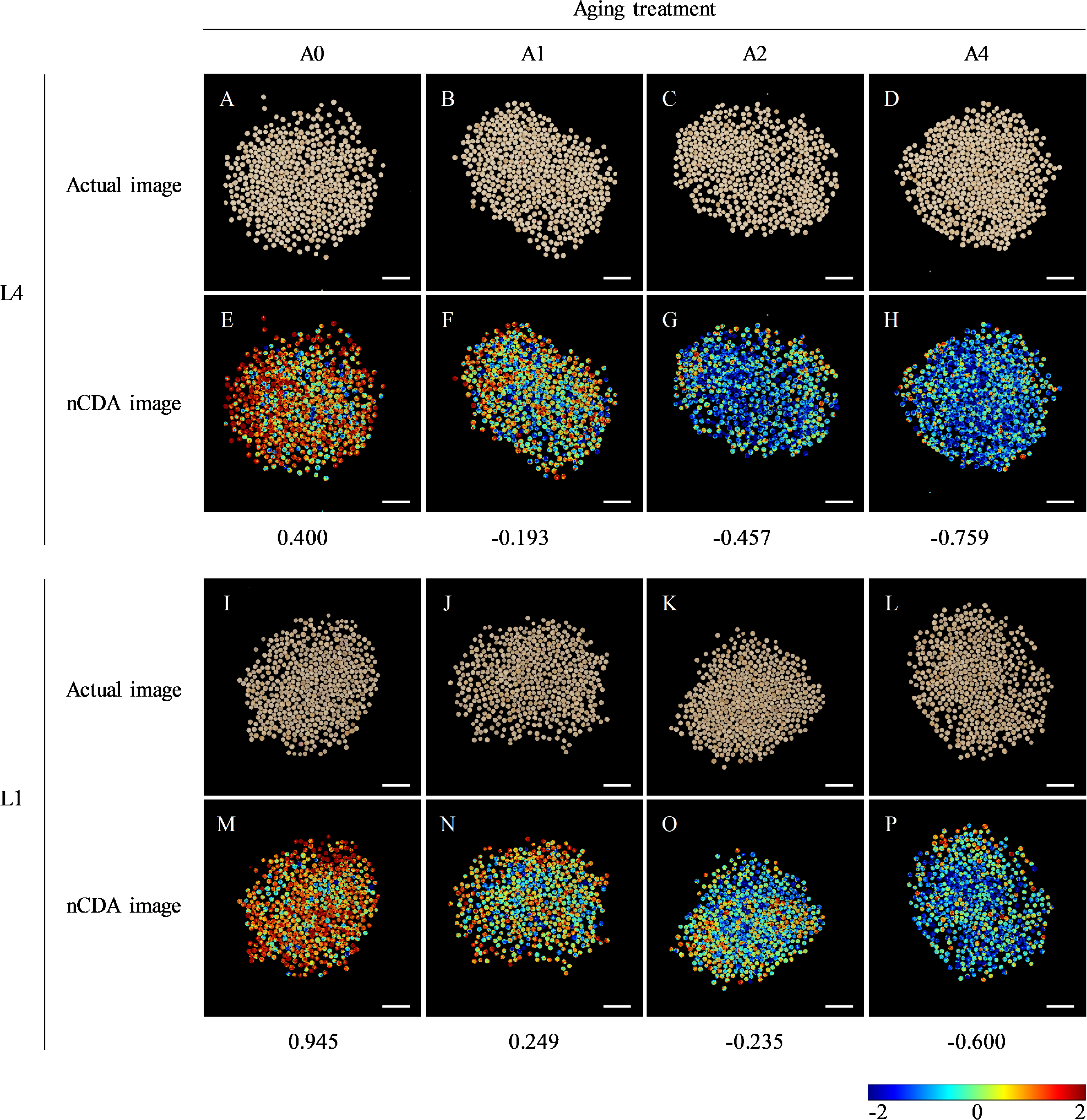 人工加速老化处理后L4和L1藜麦种子的RGB图像及对应nCDA图像。(A–D)各老化时间点L4种子的RGB图像及(E–H)对应nCDA图像。(I–L)各老化时间点L1种子的RGB图像及(M–P)对应nCDA图像。比例尺=1厘米。A0、A1、A2和A4分别表示人工加速老化时长为0、1、2和4天。在nCDA图像中,红色越深表示种子活力越高,蓝色越深表示种子活力越低。因此,红色种子越多,种子批次活力越高;蓝色种子越多,种子批次活力越低。
人工加速老化处理后L4和L1藜麦种子的RGB图像及对应nCDA图像。(A–D)各老化时间点L4种子的RGB图像及(E–H)对应nCDA图像。(I–L)各老化时间点L1种子的RGB图像及(M–P)对应nCDA图像。比例尺=1厘米。A0、A1、A2和A4分别表示人工加速老化时长为0、1、2和4天。在nCDA图像中,红色越深表示种子活力越高,蓝色越深表示种子活力越低。因此,红色种子越多,种子批次活力越高;蓝色种子越多,种子批次活力越低。
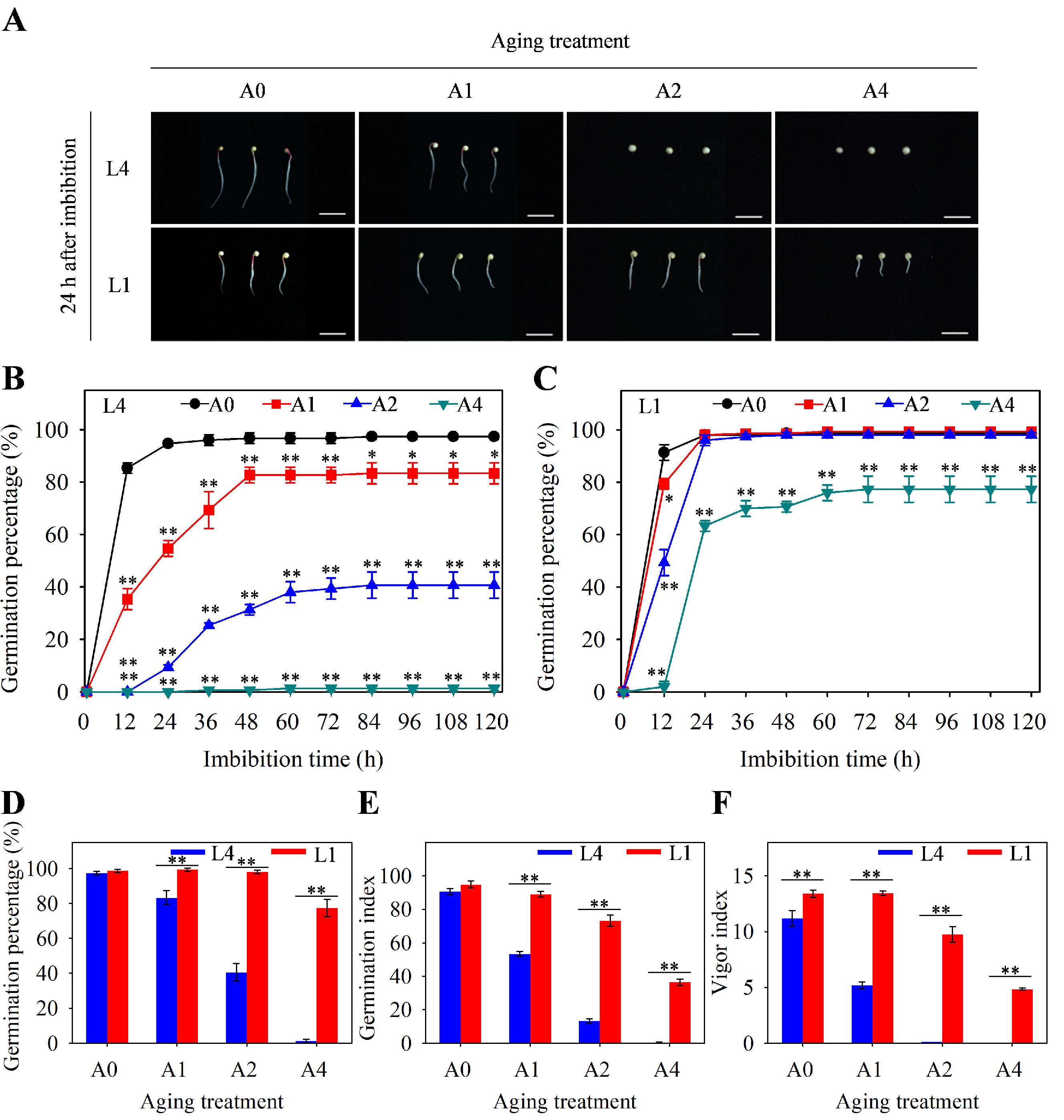 人工加速老化处理后L4和L1藜麦种子的萌发特性。(A) 种子吸水24小时后的表型萌发差异。比例尺=1厘米。(B) L4种子和(C) L1种子在120小时吸水过程中的萌发率。(D) 吸水120小时后L4和L1种子的萌发率、(E)萌发指数及(F)活力指数。数值表示为均值±标准误(n=3)。图(B)和(C)中的星号表示老化组(A1、A2和A4)与对照组(A0)之间存在显著差异,而图(D–F)中的星号表示L4和L1两个品种之间存在显著差异。*和**分别表示根据Student t检验在5%和1%水平上存在显著差异。
人工加速老化处理后L4和L1藜麦种子的萌发特性。(A) 种子吸水24小时后的表型萌发差异。比例尺=1厘米。(B) L4种子和(C) L1种子在120小时吸水过程中的萌发率。(D) 吸水120小时后L4和L1种子的萌发率、(E)萌发指数及(F)活力指数。数值表示为均值±标准误(n=3)。图(B)和(C)中的星号表示老化组(A1、A2和A4)与对照组(A0)之间存在显著差异,而图(D–F)中的星号表示L4和L1两个品种之间存在显著差异。*和**分别表示根据Student t检验在5%和1%水平上存在显著差异。
研究结论
1.多光谱成像和发芽表型证实,L1(高耐储)种子活力衰退速率显著慢于 L4(低耐储),nCDA 可视化可有效区分两品种种子活力差异:
①形态特征:老化后两品种种子颜色参数(CIELab L*、A*、B*)和饱和度显著升高,但形状参数(面积、长度等)无显著变化;L1 种子粒径显著小于 L4,且种皮颜色更深;
②nCDA 可视化:随着老化时间延长,两品种红色高活力种子占比减少,蓝色低活力种子占比增加,且各时间点 L1 的 nCDA 值均高于 L4,表明 L1 种子活力衰退更慢;
③发芽表型:A0 时两品种发芽率均达 97% 以上;A4 时 L4 发芽率降至 1%,而 L1 仍保持 77%;L1 的发芽指数和活力指数在各老化阶段均显著高于 L4。
2.转录组分析表明,L4 种子活力衰退与黄酮类生物合成、萜类骨架生物合成、TCA 循环通路基因下调密切相关;L1 通过维持碳代谢通路关键基因(如 ENO1、IDH、NADP-ME)上调,保障能量供应和解毒能力,增强耐储性;
 北京博普特科技有限公司是丹麦Videometer多光谱成像系统的中国区总代理,全面负责其系列产品在中国市场的推广、销售和售后服务。
北京博普特科技有限公司是丹麦Videometer多光谱成像系统的中国区总代理,全面负责其系列产品在中国市场的推广、销售和售后服务。